各药品生产企业及配送企业:
为满足我院临床诊疗需求,拟启动我院2024年新药遴选工作。为更好地了解市场上药品相关信息,并作为后续新药遴选的参考,现开展新药遴选市场信息调研,相关事宜公告如下:
一、新药定义
新药是指国家相关部门批准同意生产使用,且初次进入我院《基本用药目录》;在安全性、有效性、经济性等方面有显著特点,且能提升我院现有药物治疗水平的药品。
申报的品种与医院常购药品通用名相同,但规格或剂型不同的品种,视为新药。
二、新药引进原则
(一)依据安全、有效、经济的用药原则和医院疾病治疗特点,优化医院用药目录。促进基本药物优先配备使用,形成以基本药物为主导的“1+X”用药模式。“1”为国家基本药物目录;“X”为非基本药物,经医院药委会充分评估论证,优先选择国家组织集中采购药品、国家医保目录药品、国家谈判药品。
(二)医院《基本用药目录》当中,口服剂型与注射剂型各不超过“一品两规”(儿童用药剂型除外)。
三、申报基本原则
(一)属于“四川医保公共服务——药品和医用耗材招采管理系统”(以下简称平台)挂网品种。
(二)同一生产企业限报2个品规,若超额申报,所有申报视为“无效”。
(三)“中成药”只接收国药准字号为“Z”,且至少满足“国家Ⅰ类新药”“国家谈判品种”或“获得省科技进步一等奖及以上科技奖励”条件之一的品种。
(四)不接受红黄区的药品信息。
四、申报资料
生产企业或其委托的配送企业提交申请资料:
(一)《新药申请表》。
(二)生产企业提供营业执照复印件、药品生产许可证复印件。全进口药品提供全国总代理营业执照复印件、药品经营许可证复印件。所有复印件需加盖生产企业或全国总代理鲜章。
(三)平台挂网页面打印件(需显示挂网价、医保属性、红黄绿价格区间、基药属性、是否集采中选品种、是否国家谈判药品;需清晰并盖企业鲜章)。
(四)经国家食品药品监督管理局(SFDA)批准的法定药品说明书。
(五)新药申报承诺书。
(六)产品介绍资料(临床研究、临床指南等)。
(七)申报药品如系四川大学华西医院、四川大学华西第二医院、四川大学华西口腔医院及四川省人民医院在用品种,提供申报药品的配送协议或药品销售出库单。
(八)法人授权委托书(生产企业对配送企业授权)
(九)法人授权委托书(供应商对代理人授权)
五、申报要求
(一)各企业应真实、准确、规范填写资料。如资料填写不全或填写错误者,不接受更正,视为无效资料。
(二)除企业证照加盖生产企业(或全国总代理)鲜章外,余资料均加盖申报企业鲜章即可。同一类别资料页码较多者,加盖骑缝章。
(三)所有提交资料须真实有效,各类资料按要求整理汇编成册。
(四)各相关企业不得直接与临床科室及医生联系,一经核实,将取消该企业参与资格。
六、资料接收
(一)接收资料内容:
1.新药信息汇总表(附件1),接收可编辑的Excel版本。
2.新药市场调研申报书(附件2):按照附件2的顺序将资料整理,并转换为PDF版本。
(二)接收方式:
仅接收附件1和附件2的电子版资料。将上述资料发送到指定邮箱ypcgzyy@163.com。主题:药品名-剂型-规格。资料以附件形式按要求上传,如图: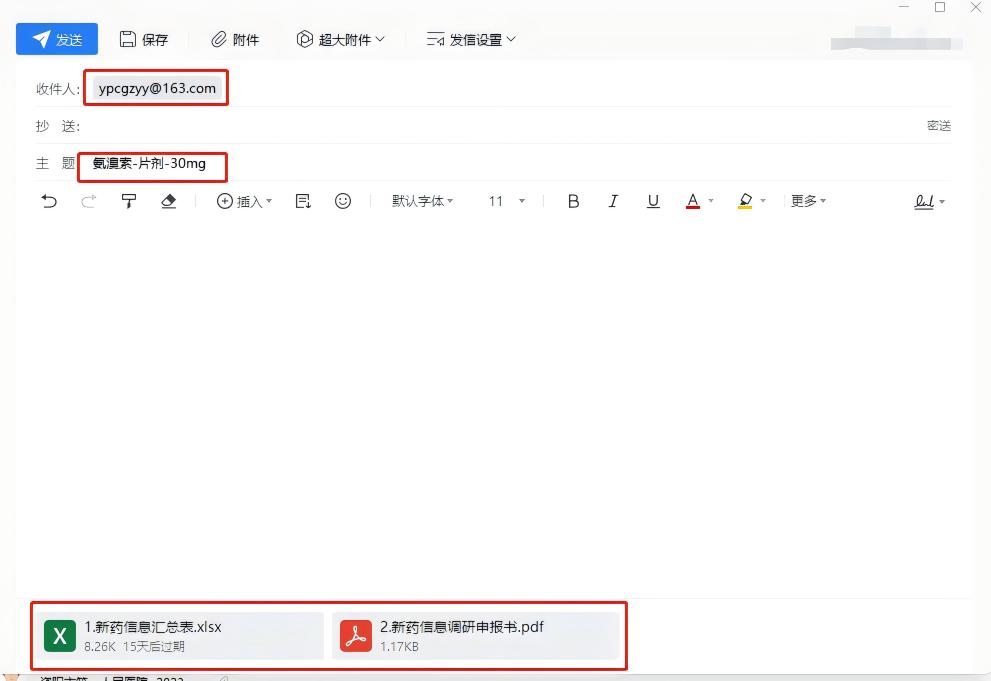
(三)接收时间:2024年10月12日-10月18日。
七、其他
(一)联系人及联系方式:黄老师,028-26578063。
(二)以上内容解释权归资阳市中心医院药事管理与药物治疗学委员会所有。
资阳市中心医院
2024年10月12日