飞行检查,3省3家医疗器械企业被停产
2017年度,国家药监总局飞行检查第二批结果出炉,有3家医疗器械生产企业均被责令立即停产。
依据药监总局4月26日所发公告,今年4月10日-12日,北京、江苏、广东的3家隐形眼镜产品生产企业进行了有因飞行检查。结果,3家企业均被发现质量管理体系存在严重缺陷,违背医械GMP相关要求。
1、北京自然美光学有限公司:停产+依法查处
产品名称:软性亲水接触镜
严重缺陷有7项,包括:抽检成品检验样本量与注册产品标准规定不符;检验记录无法追溯;部分原料的技术要求不符合现行中国药典要求;关键工序的工艺参数未进行验证和确认;不合格品未作标识与隔离等。

同时,检查中还发现企业在未经许可的地址内存放有大量包装好隐形眼镜、拆解的玻璃瓶、铝箔盖,以及旋转蒸发仪、搅拌仪等,涉嫌存在在未经许可的地址生产的行为。
药监总局要求,北京市药监局责令企业立即停产整改,并对企业存在的涉嫌违法违规行为依法查处。
2、江苏海伦隐形眼镜有限公司:停产
产品名称:软性亲水接触镜、隐形眼镜润滑液
严重缺陷有2项,包括包装材料耗用量记录无法追溯;注模工序也无法追溯等。
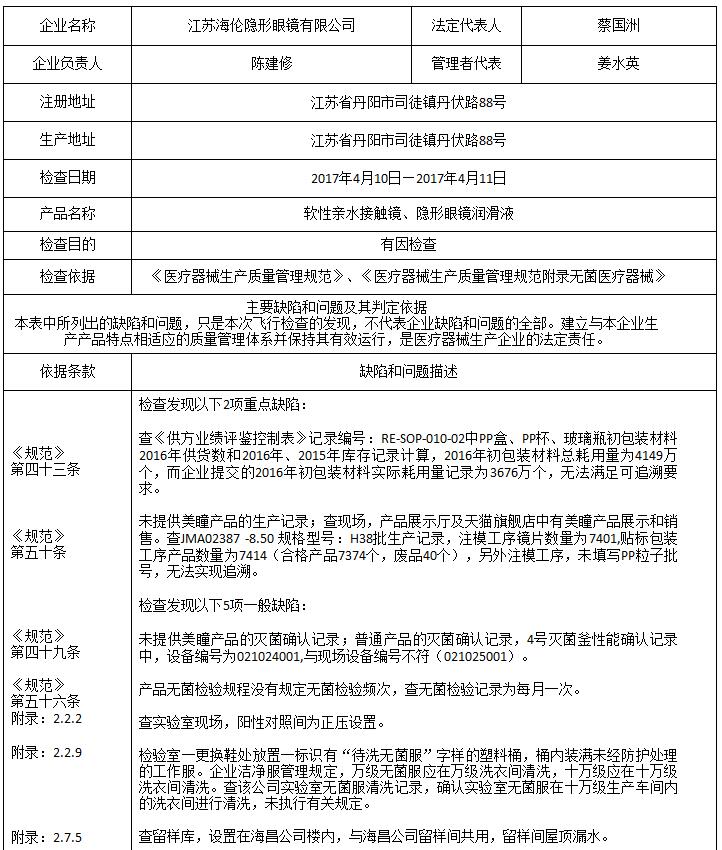

总局要求,江苏省药监局依法责令企业立即停产整改。
3、广州科甫眼镜有限公司:停产
产品名称:软性亲水接触镜
严重缺陷有8项,包括:产品具体生产日期无法查证;生产批号不一致;生产记录真实性无法证实等。
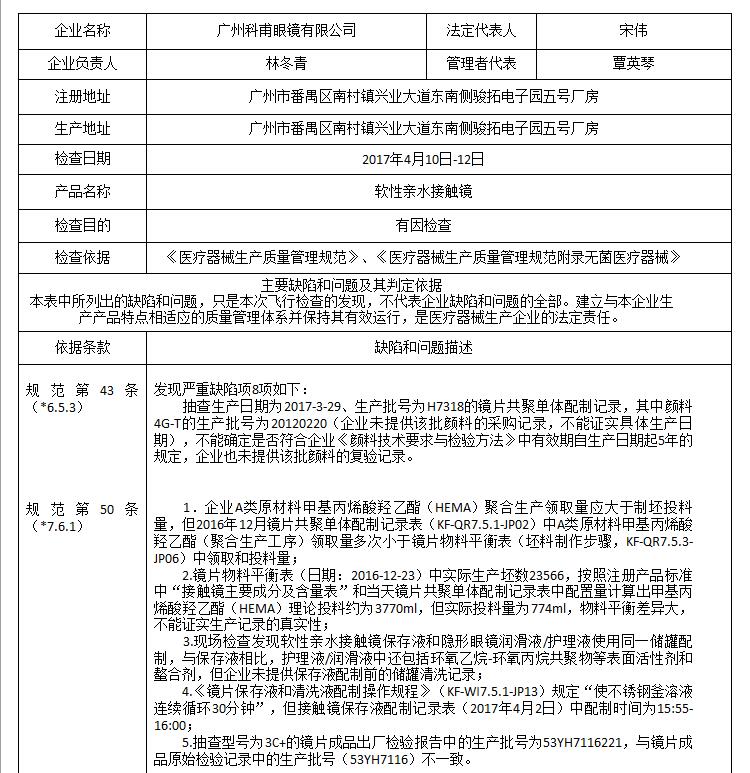


总局要求,广东省药监局依法责令企业立即停产整改。